Fitokanabinoidų neurologinės naudos apžvalga
2023 m. liepos 30 d. 11:16,
Komentarų nėra
Daugybė
fiziologinių,
psichologinių ir emocinių privalumų buvo priskirta marihuanai nuo
tada, kai pirmą kartą pranešta apie jos vartojimą 2,600 m. Pr.
Kr. Kinijos farmakopėjoje. Fitokanabinoidai,
kanabidiolis (CBD) ir delta-9-tetrahidrokanabinolis (Δ9-THC) yra
labiausiai ištirti kanapių sativa
porūšių
kanapių ir marihuanos ekstraktai. CBD ir Δ9-THC unikaliai
sąveikauja su endokanabinoidų sistema (EKS).
Tiesioginiais ir netiesioginiais veiksmais vidiniai endokanabinoidai
ir augaliniai fitokanabinoidai moduliuoja ir daro įtaką įvairioms
fiziologinėms sistemoms, kurias veikia EKS.
1980 m. Cunhair
kt.
I fazės klinikinio tyrimo metu pranešta apie prieštraukulinę
naudą 7/8 tiriamųjų, sergančių mediciniškai nekontroliuojama
epilepsija, naudojant marihuanos ekstraktus. Nuo to laiko buvo
sutelktas dėmesys į medicininę
marihuaną ir fitokanabinoidų ekstraktus. Naujausi neurologiniai
naudojimo būdai apima papildomą piktybinių smegenų navikų,
Parkinsono ligos, Alzheimerio ligos, išsėtinės sklerozės,
neuropatinio skausmo ir vaikų traukulių sutrikimų Lennox-Gastaut
ir Dravet sindromų gydymą. Be to, naudojant fitokanabinoidus
tiriami psichikos ir nuotaikos sutrikimai, tokie kaip šizofrenija,
nerimas, depresija, priklausomybė, smegenų
sukrėtimo
sindromas ir potrauminio streso sutrikimai. Fitokanabinoidai
sėkmingai
naudojami
kaip papildomas piktybinių smegenų navikų, Parkinsono ligos (PD),
Alzheimerio ligos (AD), išsėtinės sklerozės (IS), neuropatinio
skausmo ir vaikų traukulių sutrikimų, Lennox-Gastaut ir Dravet
sindromų gydymas.
Kanabinoidų
receptorių farmakologija prasidėjo 1960-ųjų pabaigoje, kai Δ9-THC
buvo izoliuotas ir susintetintas ir nustatyta, kad jis yra pagrindinė
psichoaktyvi marihuanos sudedamoji dalis.1990-ųjų pradžioje
atradus specifinius membraninius receptorius Δ9-THC, buvo nustatyta
endogeninė signalizacijos sistema, dabar žinoma kaip
endokanabinoidų sistema (ECS). Netrukus po to buvo nustatyti
endogeniniai kanabinoidai, N-arachidonoylethanolamine (anandamidas)
ir 2-arachidonoilglicerolis (2-AG). ECS susideda iš dviejų
pagrindinių tipų endogeninių G baltymų sujungtų kanabinoidų
receptorių (CB1 ir CB2), esančių žinduolių smegenyse ir visoje
centrinėje bei periferinėje nervų sistemose, įskaitant audinius,
susijusius su imunine sistema. CB1 ir CB2 receptoriai taip pat gali
egzistuoti kartu įvairiomis koncentracijomis tose pačiose vietose.
Tiek fitokanabinoidai, tiek endogeniniai kanabinoidai veikia kaip
retrogradiniai pasiuntiniai, kurie slopina grįžtamąjį ryšį tiek
sužadinančiam, tiek slopinančiam perdavimui smegenyse, aktyvuodami
presinaptinius CB1 receptorius. Manipuliuojant endokanabinoidų
degradaciniais fermentais, CB1 ir CB2 receptoriais bei jų
endogeniniais ligandais, buvo įrodyta, kad jie moduliuoja daugybę
procesų, susijusių su neurodegeneracinėmis ligomis, vėžiu,
epilepsija ir trauminiu smegenų pažeidimu. Be to, žinoma, kad ECS
daro įtaką neuroplastiškumui, apoptozei, ekscitotoksiškumui,
neuroinflammacijai ir smegenų kraujagyslių irimui, susijusiam su
insultu ir trauma.
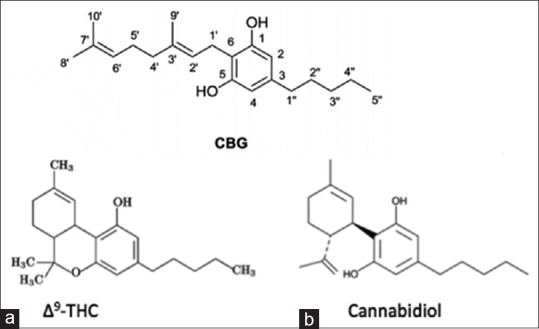
Be fitokanabinoido Δ9-THC, apskaičiuota, kad kanapių augalą sudaro daugiau kaip 400 cheminių subjektų, iš kurių daugiau kaip 60 yra fitokanabinoidiniai junginiai. Nustatyta, kad kai kurie iš šių junginių atskirai ir vienu metu unikaliai veikia ir CB1, ir CB2 receptorius ir (arba) slopina ar aktyvina receptorių funkcijas. CBD, kaip ir Δ9-THC, yra pagrindinis fitokanabinoidas, sudarantis iki 40% augalo ekstrakto. CBD pirmą kartą buvo atrastas 1940 m., Daugiau nei 20 metų prieš Δ9-THC. Dar visai neseniai kanapių tyrimuose dominavo Δ9-THC. Visos marihuanoje ir kanapėse randamų fitokanabinoidų junginių klasės, įskaitant Δ9-THC ir CBD, yra gaunamos iš įvairių kanabigerolio tipo junginių bazinės molekulinės struktūros pokyčių
Fitokanabinoidų junginiai ir ekstraktai gali būti gaunami tiek iš kanapių, tiek iš marihuanos porūšių, įskaitant CBD. CBD nesukelia tokio paties psichoaktyvaus poveikio, kaip matyti naudojant Δ9-THC (t. Y. CBD vartotojai nesijaučia euforiški). Įvairūs psichoaktyvūs poveikiai, paprastai susiję su Δ9-THC, priskiriami CB1 kanabinoidų receptorių, kurių gausu smegenyse, aktyvacijai. CB1 receptoriai turi didžiausią tankį bazinių ganglijų nutekėjimo branduoliuose, substantia nigra pars reticulata (SNr) ir vidiniuose bei išoriniuose globus pallidus segmentuose (smegenų dalis, reguliuojanti savanorišką judėjimą). Hipokampas, ypač dentato gyrus, ir smegenėlės taip pat turi didesnį CB1 receptorių tankį. Smegenų kamiene randama labai nedaug CB1 receptorių. Šios vietos rodo CB1 receptorių dalyvavimą moduliuojant atmintį, emocijas, skausmą ir judėjimą. Įrodyta, kad Δ9-THC, nukreiptas į CB1 receptorius, sumažina nociceptiją gyvūnų ūminio, visceralinio, uždegiminio ir lėtinio skausmo modeliuose. Pacientų tyrimuose su lėtiniu skausmu ir neuropatiniu skausmu marihuanos ar kanabinoidų ekstraktų vartojimas sukėlė teigiamus ir pagerėjusius simptomus.
Neuronų CB1 receptorių aktyvinimas slopina adenilo ciklazę ir sumažina neurotransmiterių išsiskyrimą blokuodamas įtampos valdomus kalcio kanalus. Šių signalizavimo kelių aktyvavimas CB1 receptoriais ir didelis šių receptorių kiekis presinaptiniuose terminaluose rodo, kad CB1 receptorių endokanabinoidinė stimuliacija slopina neuronų jaudrumą ir slopina neurotransmisiją. Dėl šių poveikių buvo tiriami fitokanabinoidai epilepsijai gydyti. Keletas farmacijos kompanijų bando sukurti sintetinius didelio afiniteto CB1 antagonistus ir atvirkštinius agonistus kaip terapinius vaistus diabetui, metaboliniam sindromui ir priklausomybei nuo narkotikų.CB2 receptoriai
CB2 receptoriai, skirtingai nei CB1, nėra labai išreikšti centrinėje nervų sistemoje (CNS). Δ9-THC poveikis imuninei funkcijai buvo priskirtas CB2 kanabinoidų receptorių sąveikai, daugiausia randamai imuninėse ląstelėse. CB2 receptoriai yra plačiai pasiskirstę pagrindiniuose imuninių ląstelių gamybos ir reguliavimo audiniuose, įskaitant blužnį, tonziles ir užkrūčio liauką. Šios ląstelių linijos apima B ir T limfocitus, natūralias žudikų ląsteles, monocitus, makrofagus, mikroglijos ląsteles ir putliąsias ląsteles. Kaip ir CB1 receptoriai, endokanabinoidų stimuliacija slopina CB2 receptorių neurotransmisiją.
Kultivuotų mikroglijos ląstelių tyrimas parodė, kad c-interferoną ir granulocitų makrofagų kolonijas stimuliuojantį faktorių (GM-CSF), žinomą kaip mikroglijos ląstelių uždegiminio atsako aktyvatorius, lydėjo reikšmingas CB2 receptorių reguliavimas. Tai rodo, kad CB2 receptoriai vaidina svarbų vaidmenį mikroglijos ląstelių funkcijoje CNS uždegiminiame atsake. CB2 aktyvinimas buvo susijęs su keliomis neurodegeneracinėmis ligomis, tokiomis kaip Huntingtono (HD) ir AD.Padidėjusi CB2 ekspresija smegenyse buvo patvirtinta naudojant CB2 selektyvias pozitronų emisijos tomografijos (PET) atsekamąsias medžiagas Alzheimerio pelių modeliuose. Ši padidėjusi ekspresija buvo susijusi su amiloido-beta plokštelių formavimu, o tai rodo galimą CB2 PET atsekamųjų medžiagų, kaip diagnostinio metodo nustatant neuroinflammacijos pradžią, naudingumą. CBD sąveika su CB2 receptoriais yra sudėtingesnė, tačiau, kaip ir Δ9-THC, manoma, kad CBD sumažina uždegiminį atsaką. CBD poveikis CB2 receptoriui yra tik vienas iš kelių būdų, kuriais CBD gali paveikti neuroinflammaciją . Kadangi tiek CBD, tiek Δ9-THC moduliuoja G baltymų sujungtų receptorių, susijusių su endokanabinoidų sistema, aktyvumą, o CBD gali veikti kaip dalinis agonistas ir antagonizuoja Δ9-THC, CBD didesnėmis dozėmis tam tikru mastu gali neutralizuoti psichoaktyvų Δ9-THC poveikį. Šį poveikį pastebi daugelis kanapių vartotojų, kurie kartu vartoja CBD.
Skirtingai nuo psichoaktyviųjų savybių, susijusių su Δ9-THC, įrodyta, kad CBD turi labai mažą toksiškumą žmonėms ir kitoms rūšims. Prarytas ir absorbuojamas CBD greitai pasiskirsto ir dėl savo lipofilinio pobūdžio gali lengvai praeiti kraujo ir smegenų barjerą. Galutinis CBD pusinės eliminacijos laikas yra apie 9 val. ir pirmiausia išsiskiria su šlapimu kaip laisva ir gliukuronido forma.
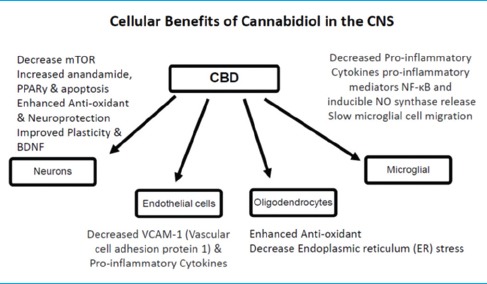
CBD tyrimai su gyvūnų modeliais ir žmonėmis parodė daugybę terapinių savybių smegenų funkcijai ir apsaugai, tiek tiesiogiai veikiant ECS, tiek darant įtaką endogeniniams kanabinoidams. Apskritai, CBD parodė anksiolitinę, antidepresantinę, neuroprotekcinę priešuždegiminę ir imunomoduliacinę naudą. CBD sumažina uždegiminių citokinų gamybą, daro įtaką mikroglijos ląstelėms, kad jos grįžtų į ramią būseną, išsaugo smegenų kraujotaką išeminių įvykių metu ir sumažina kraujagyslių pokyčius bei neuroinflammaciją. Kitas CBD poveikis yra kalcio pernašos per membranas slopinimas, anandamido įsisavinimo ir fermentinės hidrolizės slopinimas bei indukuojamo NO sintazės baltymo ekspresijos ir branduolinio faktoriaus (NF)-κB aktyvacijos slopinimas. CBD padidina smegenų adenozino kiekį, sumažindamas adenozino reabsorbciją. Padidėjęs adenozinas yra susijęs su neuroprotekcija ir sumažėjusiu uždegimu po smegenų traumos. Taip pat žinoma, kad CBD daro poveikį kraujagyslėms, sukelia vazodilataciją, taip pat hipotenziją, kuri gali būti naudinga kaip apsauga nuo smegenų kraujagyslių pažeidimo, susijusio su insultu. CBD turi keletą savybių, kurios gali būti naudojamos AD gydymui, įskaitant glutamato sukelto sužadinimo prevenciją, uždegimą skatinančių mediatorių mažinimą ir gebėjimą pašalinti reaktyvias deguonies rūšis (ROS) ir sumažinti lipidų peroksidaciją. Eksperimentiškai, in vitro, kanabinoidų receptorių sąveika su CBD ir Δ9-THC, kartu ir atskirai, parodė neuronų apsaugą nuo sužadinimo, hipoksijos ir gliukozės trūkumo; In vivo kanabinoidai mažina hipokampo neuronų praradimą ir infarkto tūrį po smegenų išemijos, ūminės smegenų traumos ir sukelto ekscitotoksiškumo. Šis poveikis buvo priskirtas glutamato perdavimo slopinimui, kalcio antplūdžio sumažėjimui, sumažėjusiam mikroglijos aktyvavimui ir vėlesniam kenksmingų kaskadų slopinimui, pvz., Naviko nekrozės faktoriaus-alfa generavimui ir oksidaciniam stresui. Taip pat įrodyta, kad Δ9-THC apsaugo smegenis nuo įvairių neuronų pažeidimų ir pagerina neurodegeneracijos simptomus gyvūnų modeliuose MS, PD, HD, amiotrofinė šoninė sklerozė (ALS) ir AD. Kaip ir CBD, Δ9-THC gali pasiūlyti ne ECS apsaugą tiesioginiu poveikiu neuronų ląstelėms ir neneuroniniams elementams smegenyse. Mechanizmai apima sužadinimo glutamaterginių transmisijų ir sinapsinio plastiškumo moduliavimą, imuninio atsako moduliavimą, priešuždegiminių mediatorių išsiskyrimą, N-metil-D-aspartato receptorių jaudrumo moduliavimą ir jo poveikį tarpų sankryžoms, kalciui ir antioksidantams. AD būdingas padidėjęs beta-amiloido peptidų nusėdimas kartu su glialų aktyvacija senatvinėse plokštelėse, selektyvus neuronų praradimas ir pažinimo deficitas. Kanabinoidai yra neuroprotekciniai nuo ekscitotoksiškumo in vitro ir pacientams, sergantiems ūminiu smegenų pažeidimu. AD sergantiems žmonėms ląsteliniai senilinių plokštelių tyrimai parodė kanabinoidų receptorių CB1 ir CB2 ekspresiją kartu su mikroglijos aktyvacijos žymenimis. Tačiau kontrolinių CB1 teigiamų neuronų yra daugiau, palyginti su AD mikroglijos aktyvacijos sritimis. AD smegenyse taip pat pastebimai sumažėjo G-baltymų receptorių jungtis ir CB1 receptorių baltymų ekspresija. Paprastai manoma, kad aktyvuotas mikroglijos klasteris senatvinėse plokštelėse yra atsakingas už vykstantį uždegiminį ligos procesą.Šaltinis: Fitokanabinoidų neurologinės naudos apžvalga - PMC (nih.gov)