CBD naudojimas spazmams gydyti
2024-02-01,
Komentarų nėra
Klinikiniai
tyrimai
patvirtina ilgalaikį tetrahidrokanabinolio ir kanabidiolio (THC:CBD)
veiksmingumą, siekiant pagerinti išsėtine skleroze (IS) sergančių
pacientų, atsparių kitiems vaistams, spazmiškumą. Šis tyrimas
buvo pristatytas 2019 m. Amerikos neurologijos akademijos metiniame
susitikime, vykusiame gegužės 4–10 d. Filadelfijoje.
Šio
stebėjimo, perspektyvaus, daugiacentrio tyrimo tyrėjai siekė
įvertinti realaus gyvenimo, ilgalaikio THC:CBD veiksmingumo
rezultatus gydant didelę Italijos pacientų populiaciją, sergančią
gydymui atspariu IS spazmiškumu. Spastiškumas buvo įvertintas
naudojant skaitmeninę
vertinimo skalę (0–10) pradžioje, 1 mėnesį, 6 mėnesius, 12
mėnesių ir 18 mėnesių nuo gydymo pradžios.
Po
vieno mėnesio 1502 (81,4 %) iš 1845 pacientų spastiškumo
skaitmeninėje skalėje pagerėjo ≥ 20 %, o 814 (40,2 %) pagerėjo
≥ 30 %. Spastiškumo balų vidurkis sumažėjo 28,9 % 1 mėnesį ir
36,8 % 18 mėnesį. Iš viso 727 (39,4 %) dalyviai nutraukė gydymą:
388 pranešė apie veiksmingumo trūkumą, o 339 patyrė
nepageidaujamų reiškinių. Dažniausi nepageidaujami reiškiniai
buvo galvos svaigimas (37,5 %), mieguistumas (34,8 %), nuovargio
padidėjimas
(28,3 %) ir pažinimo simptomai (15,9 %). Atliekant daugiamatę
analizę, pacientai, kurių pradinis spastiškumo balas buvo didesnis
(šansų santykis 2,21; 95 % PI, 1,12–6,28; P < 0,01) arba
didesnis balų pokytis nuo pradinio iki 1 mėnesio (šansų santykis
2,03; 95 % PI, 1,04). -8,14; P <,05) buvo dvigubai didesnė
tikimybė tęsti gydymą ilgiau nei 18 mėnesių.
Tyrėjai
teigia, kad šie rezultatai patvirtina THC:CBD terapijos
veiksmingumą, siekiant sumažinti gydymui atsparų IS spazmiškumą
ir palaikyti pagerėjimą 18 mėnesių.
Rekomenduojamas pilno spektro cbd aliejus.
Kanabinoidų dozavimas neurologijoje
2023-08-25,
Komentarų nėra
Kiekvieno žmogaus organizmas skirtingai reaguoja į kanabinoidus,
todėl CBD dozavimą pradėkite nuo startinės dozės, kuri yra 0,5mg
CBD kilogramui kūno svorio. Stebėkite kaip CBD veikia ir, esant
reikalui, dozę padidinkite arba sumažinkite, kol pasieksite norimą
efektą.
Kaip tai atrodo praktikoje? Jeigu sveriate 100 kg, tuomet
startinė paros dozė bus 50mg CBD (nepainioti su mililitrais).
Kanabinoidai metabolizuojami (suskaidomi) per 8-10 valandų.
Vadinasi, jeigu norite poveikio visą parą, tuomet reikės vartoti
du kartus dienoje, po 25mg. Jeigu Jums reikia stipresnio poveikio
nakties metu, tuomet naudokite 50mg vakare. Kaip jau minėjau, tai
startinė dozė. Jums tinkančią dozę atsititruosite su laiku.
In vivo Įrodymai apie kanabidiolio (CBD) terapines savybes Alzheimerio ligai gydyti
2023-07-31,
Komentarų nėra
Alzheimerio liga (AD) yra sekinanti neurodegeneracinė liga, kuria serga vis daugiau žmonių. Jai būdingas amiloido β ir tau hiperfosforilinimo kaupimasis, taip pat neuroinflammacija ir oksidacinis stresas. Dabartiniai AD gydymo būdai nesustabdo ir nepakeičia ligos progresavimo, pabrėždami naujų, veiksmingesnių gydymo būdų poreikį. Kanabidiolis (CBD) yra ne psichoaktyvus fitokanabinoidas, kuris in vitro parodė neuroprotekcines, priešuždegimines ir antioksidacines savybes. Taigi jis tiriamas kaip galimas daugiafunkcinis AD gydymo būdas. Čia apibendriname dabartinį CBD poveikio in vivo status quo nusistovėjusiuose AD farmakologiniuose ir transgeniniuose gyvūnų modeliuose. Tyrimai rodo CBD gebėjimą sumažinti reaktyvią gliozę ir neuroinflammacinį atsaką, taip pat skatinti neurogenezę. Svarbu tai, kad CBD taip pat panaikina ir neleidžia vystytis kognityviniam deficitui AD. Įdomu tai, kad kombinuotos CBD ir Δ terapijos9-tetrahidrokanabinolis (THC), pagrindinė kanapių sativa veiklioji medžiaga, rodo, kad CBD gali slopinti psichoaktyvų poveikį, susijusį su THC, ir galbūt tarpininkauti didesnei terapinei naudai nei vien tik fitokanabinoidas. Tyrimai pateikia "principinį įrodymą", kad CBD ir galbūt CBD-THC deriniai yra tinkami kandidatai į naujas AD terapijas.
Problema
Alzheimerio liga (AD) yra sekinanti neurodegeneracinė liga, kuriai būdingas kognityvinis nuosmukis. Tai yra labiausiai paplitusi demencijos forma, sudaranti daugiau nei 60% atvejų ir paveikianti daugiau nei 33 milijonus žmonių visame pasaulyje (Wisniewski ir Goni, 2014; Alzheimerio asociacija, 2015). Deja, dėl senėjančios visuomenės tikimasi, kad iki 115 m. šis skaičius pasieks 2050 milijonų (Wisniewski ir Goni, 2014). AD paprastai prasideda nuo nedidelio trumpalaikės atminties, mokymosi, bendravimo ir erdvinės orientacijos deficito. Vidutinio sunkumo ligos stadijoje deficitas pradeda daryti įtaką kasdieniam gyvenimui, įskaitant valgymą, apsirengimą ir emocinę kontrolę (Alzheimerio asociacija, 2015). Vėlyvose ligos stadijose yra visuotinis kognityvinių gebėjimų sutrikimas, turintys sunkių kalbos ir veido atpažinimo sutrikimų, dėl kurių pacientams reikia 24 valandų priežiūros. Ligai progresuojant, pacientai tampa vis imlesni ir kitoms ligoms (Alzheimerio asociacija, 2015).
Kilmė
AD skirstoma į dvi rūšis: vėlyvos pradžios sporadinę AD (>95% atvejų) arba ankstyvos pradžios šeiminę AD (<5% atvejų) (Gotz ir Ittner, 2008). Nors sporadinė AD yra labiausiai paplitusi forma, ji yra daug mažiau suprantama nei šeiminė AD. Šeimos AD taip pat žinoma kaip genetinė forma, nes ji atsiranda dėl autosominių dominuojančių mutacijų amiloido pirmtako baltymo (APP) gene arba presenilino 1 ir 2 (PS1 ir PS2) genuose (Gotz ir Ittner, 2008; Bettens ir kt., 2013). APP yra pirmtako molekulė, kuri yra suskaidyta į amiloido β (Aβ) peptidus, o PS1 ir PS2 koduoja γ sekretazės ir β sekretazės kompleksus, kurie tarpininkauja APP susiliejimui (Bettens et al., 2013; Gotz ir Ittner, 2008). Po APP sujungimo Aβ gali egzistuoti dviem formomis: Aβ40 ir Aβ42. Aβ42 manoma, kad tai yra toksiškesnė baltymo forma, nes jis kaupiasi lengviau nei Aβ40 (Chapman ir kt., 2001). Sporadinio AD priežastis yra ne tokia aiški ir dar turi būti apibrėžta, tačiau naujausi tyrimai rodo, kad ji gali atsirasti dėl sudėtingos sąveikos tarp kelių aplinkos veiksnių ir įvairių jautrių genų. Buvo pranešta, kad daugybė genų yra jautrūs atsitiktinės AD genai, o geriausiai dokumentuotas yra APOE (Kamboh, 2004).
Nors šeiminė ir sporadinė AD skiriasi savo priežastimi, ligos progresavimas nuo šio momento atrodo toks pat. Abi AD formos pasižymi neurodegeneracine kaskada, kurią, atrodo, skatina Aβ (besiformuojančios senatvinės plokštelės) ir hiperfosforilintos tau [formuojančios neurofibriliniai raizginiai (NFT)] kaupimasis (Chapman et al., 2001). Kaskada sukelia neuroinflammaciją ir oksidacinį stresą, kuris sukuria neurotoksinę aplinką, kuri stiprina neurodegeneraciją ir galiausiai sukelia kognityvinį nuosmukį (Hardy ir Selkoe, 2002; Ahmed ir kt., 2015). Be to, Aβ sukelta neurodegeneracija padidina glutamato kiekį AD pacientų smegenų stuburo skystyje (Pomara ir kt., 1992), o cholinerginiai neuronai prarandami smegenų srityse, svarbiose atminties apdorojimui (ir kartu su acetilcholino sumažėjimu) (Schliebs ir Arendt, 2011).
Dabartiniai gydymo būdai
Nepaisant to, kad mes geriau suprantame ligos mechanizmą, dabartiniai patvirtinti AD gydymo būdai teikia tik ribotą terapinę naudą. Yra keturi patvirtinti vaistai, trys yra acetilcholinesterazės inhibitoriai (rivistagminas, donepezilis ir galantaminas) ir vienas yra N-metil-D-aspartato (NMDA) receptorių antagonistas (memantinas) (Mangialasche ir kt., 2010). Deja, visi jie buvo susiję su neigiamu poveikiu. Acetilcholinesterazės inhibitoriai gali sukelti pykinimą, vėmimą, viduriavimą ir svorio kritimą (Kaduszkiewicz et al., 2005), o žinoma, kad memantinas sukelia haliucinacijas, galvos svaigimą ir nuovargį (Herrmann ir kt., 2011). Be to, nė vienas iš šių gydymo būdų neužkerta kelio ligos progresavimui ar jo nepanaikina, o ligos simptomus gydo ribotai veiksmingai (Salomone et al., 2012).
Dabartiniai klinikiniai tyrimai, skirti įvertinti naujus AD gydymo būdus, yra skirti įvairiems AD patologijos aspektams, daug dėmesio skiriant Aβ. Klinikiniuose tyrimuose buvo tiriami tiek β, tiek γ sekretazės inhibitoriai, kurie vaidina lemiamą vaidmenį formuojant patologinį Aβ. Deja, β sekretas sunku nustatyti, o γ sekretazės turi daugybę funkcijų, dėl kurių atsiranda neigiamas šalutinis poveikis (pvz., sutrikęs pažinimas ir funkcionalumas, toksinis poveikis virškinimo traktui ir padidėjęs odos vėžio dažnis) (Imbimbo ir Giardina, 2011; Schenk ir kt., 2012). Taip pat buvo tiriama aktyvi ir pasyvi imunoterapija, nukreipta į senatvines plokšteles ir NFT. Aβ imunoterapija pelių modeliuose parodė potencialą, nes padidino Aβ mikroglijos fagocitozę ir sumažino kognityvinį nuosmukį. Tačiau II ir III fazės klinikiniuose tyrimuose šie gydymo būdai parodė ribotą veiksmingumą arba sukėlė sunkų nepageidaujamą poveikį (pvz., Meningoenchephalitis) (Mullane ir Williams, 2013). Neseniai atliktas tyrimas, kuriame buvo tiriama antikūnais pagrįsta Aβ imunoterapija, parodė daug žadančius rezultatus I ir II fazės tyrimuose, tačiau ši terapija dar turi būti atlikta III fazės klinikiniuose tyrimuose (Sevigny et al., 2016). Tau imunoterapija buvo veiksminga AD pelių modeliuose, tačiau klinikinių tyrimų metu ji buvo nelabai sėkminga (McGeer et al., 2006; Schenk ir kt., 2012; Mullane ir Williams, 2013).
Epidemiologiniai duomenys parodė, kad nesteroidiniai vaistai nuo uždegimo (NVNU) yra susiję su sumažėjusia AD rizika (McGeer et al., 2006). Be to, tyrimai su gyvūnais parodė, kad gydymas NVNU gali susilpninti AD patogenezę, o tai rodo, kad neuroinflammacijos slopinimas gali sulėtinti AD progresavimą (Maccioni et al., 2009). Tačiau NVNU taip pat buvo susiję su sunkiu ilgalaikiu neigiamu poveikiu (pvz., virškinimo trakto problemomis) ir parodė tik ribotą veiksmingumą mažinant klinikinius simptomus arba užkertant jiems kelią (McGeer et al., 2006; Rojo ir kt., 2008).
Mažai tikėtina, kad bet koks vaistas, veikiantis vienu keliu ar taikiniu, sušvelnins sudėtingą patoetiologinę kaskadą, sukeliančią AD. Todėl daugiafunkcinis vaistų metodas, nukreiptas į keletą AD patologijų vienu metu, suteiks geresnės, platesnės naudos nei dabartiniai terapiniai metodai (Van der Schyf ir Geldenhuys, 2011; Bedse ir kt., 2015). Svarbu tai, kad endokanabinoidų sistema neseniai atkreipė dėmesį į AD tyrimus, nes ji yra susijusi su įvairių procesų, susijusių su AD, reguliavimu, įskaitant oksidacinį stresą (Marsicano ir kt., 2002), glijos ląstelių aktyvaciją (Germain ir kt., 2002) ir makromolekulių klirensą (Bilkei-Gorzo, 2012).
Kanabidiolis
Fitokanabinoidinis kanabidiolis (CBD) yra pagrindinis kandidatas į šią naują gydymo strategiją. In vitro nustatyta, kad CBD yra neuroprotekcinis (Esposito ir kt., 2006b), siekiant užkirsti kelią hipokampo ir žievės neurodegeneracijai (Hamelink ir kt., 2005), turėti priešuždegiminių ir antioksidacinių savybių (Mukhopadhyay ir kt., 2011), sumažinti tau hiperfosforilinimą (Esposito ir kt., 2006a) ir reguliuoti mikroglijos ląstelių migraciją (Walter et al., 2003; Martín-Moreno ir kt., 2011). Be to, buvo įrodyta, kad CBD apsaugo nuo Aβ sukelto neurotoksiškumo ir mikroglijos aktyvuoto neurotoksiškumo (Janefjord et al., 2014), mažina Aβ gamybą, skatindamas APP ubikiaciją (Scuderi et al., 2014) ir gerina ląstelių gyvybingumą (Harvey et al., 2012) (apibendrinta 1 lentelėje). Šios savybės rodo, kad CBD yra puikiai pritaikytas gydyti daugybę patologijų, paprastai randamų AD.
Fitokanabinoidų neurologinės naudos apžvalga
2023-07-30,
Komentarų nėra
Daugybė
fiziologinių,
psichologinių ir emocinių privalumų buvo priskirta marihuanai nuo
tada, kai pirmą kartą pranešta apie jos vartojimą 2,600 m. Pr.
Kr. Kinijos farmakopėjoje. Fitokanabinoidai,
kanabidiolis (CBD) ir delta-9-tetrahidrokanabinolis (Δ9-THC) yra
labiausiai ištirti kanapių sativa
porūšių
kanapių ir marihuanos ekstraktai. CBD ir Δ9-THC unikaliai
sąveikauja su endokanabinoidų sistema (EKS).
Tiesioginiais ir netiesioginiais veiksmais vidiniai endokanabinoidai
ir augaliniai fitokanabinoidai moduliuoja ir daro įtaką įvairioms
fiziologinėms sistemoms, kurias veikia EKS.
1980 m. Cunhair
kt.
I fazės klinikinio tyrimo metu pranešta apie prieštraukulinę
naudą 7/8 tiriamųjų, sergančių mediciniškai nekontroliuojama
epilepsija, naudojant marihuanos ekstraktus. Nuo to laiko buvo
sutelktas dėmesys į medicininę
marihuaną ir fitokanabinoidų ekstraktus. Naujausi neurologiniai
naudojimo būdai apima papildomą piktybinių smegenų navikų,
Parkinsono ligos, Alzheimerio ligos, išsėtinės sklerozės,
neuropatinio skausmo ir vaikų traukulių sutrikimų Lennox-Gastaut
ir Dravet sindromų gydymą. Be to, naudojant fitokanabinoidus
tiriami psichikos ir nuotaikos sutrikimai, tokie kaip šizofrenija,
nerimas, depresija, priklausomybė, smegenų
sukrėtimo
sindromas ir potrauminio streso sutrikimai. Fitokanabinoidai
sėkmingai
naudojami
kaip papildomas piktybinių smegenų navikų, Parkinsono ligos (PD),
Alzheimerio ligos (AD), išsėtinės sklerozės (IS), neuropatinio
skausmo ir vaikų traukulių sutrikimų, Lennox-Gastaut ir Dravet
sindromų gydymas.
Kanabinoidų
receptorių farmakologija prasidėjo 1960-ųjų pabaigoje, kai Δ9-THC
buvo izoliuotas ir susintetintas ir nustatyta, kad jis yra pagrindinė
psichoaktyvi marihuanos sudedamoji dalis.1990-ųjų pradžioje
atradus specifinius membraninius receptorius Δ9-THC, buvo nustatyta
endogeninė signalizacijos sistema, dabar žinoma kaip
endokanabinoidų sistema (ECS). Netrukus po to buvo nustatyti
endogeniniai kanabinoidai, N-arachidonoylethanolamine (anandamidas)
ir 2-arachidonoilglicerolis (2-AG). ECS susideda iš dviejų
pagrindinių tipų endogeninių G baltymų sujungtų kanabinoidų
receptorių (CB1 ir CB2), esančių žinduolių smegenyse ir visoje
centrinėje bei periferinėje nervų sistemose, įskaitant audinius,
susijusius su imunine sistema. CB1 ir CB2 receptoriai taip pat gali
egzistuoti kartu įvairiomis koncentracijomis tose pačiose vietose.
Tiek fitokanabinoidai, tiek endogeniniai kanabinoidai veikia kaip
retrogradiniai pasiuntiniai, kurie slopina grįžtamąjį ryšį tiek
sužadinančiam, tiek slopinančiam perdavimui smegenyse, aktyvuodami
presinaptinius CB1 receptorius. Manipuliuojant endokanabinoidų
degradaciniais fermentais, CB1 ir CB2 receptoriais bei jų
endogeniniais ligandais, buvo įrodyta, kad jie moduliuoja daugybę
procesų, susijusių su neurodegeneracinėmis ligomis, vėžiu,
epilepsija ir trauminiu smegenų pažeidimu. Be to, žinoma, kad ECS
daro įtaką neuroplastiškumui, apoptozei, ekscitotoksiškumui,
neuroinflammacijai ir smegenų kraujagyslių irimui, susijusiam su
insultu ir trauma.
Be fitokanabinoido Δ9-THC, apskaičiuota, kad kanapių augalą sudaro daugiau kaip 400 cheminių subjektų, iš kurių daugiau kaip 60 yra fitokanabinoidiniai junginiai. Nustatyta, kad kai kurie iš šių junginių atskirai ir vienu metu unikaliai veikia ir CB1, ir CB2 receptorius ir (arba) slopina ar aktyvina receptorių funkcijas. CBD, kaip ir Δ9-THC, yra pagrindinis fitokanabinoidas, sudarantis iki 40% augalo ekstrakto. CBD pirmą kartą buvo atrastas 1940 m., Daugiau nei 20 metų prieš Δ9-THC. Dar visai neseniai kanapių tyrimuose dominavo Δ9-THC. Visos marihuanoje ir kanapėse randamų fitokanabinoidų junginių klasės, įskaitant Δ9-THC ir CBD, yra gaunamos iš įvairių kanabigerolio tipo junginių bazinės molekulinės struktūros pokyčių
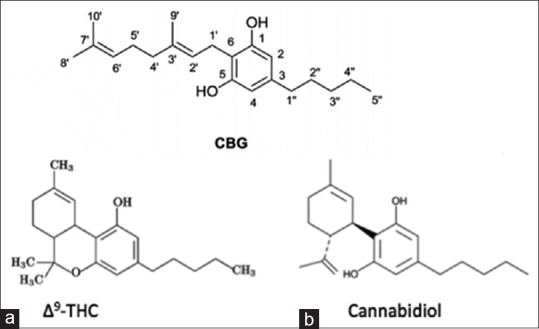
Fitokanabinoidų junginiai ir ekstraktai gali būti gaunami tiek iš kanapių, tiek iš marihuanos porūšių, įskaitant CBD. CBD nesukelia tokio paties psichoaktyvaus poveikio, kaip matyti naudojant Δ9-THC (t. Y. CBD vartotojai nesijaučia euforiški). Įvairūs psichoaktyvūs poveikiai, paprastai susiję su Δ9-THC, priskiriami CB1 kanabinoidų receptorių, kurių gausu smegenyse, aktyvacijai. CB1 receptoriai turi didžiausią tankį bazinių ganglijų nutekėjimo branduoliuose, substantia nigra pars reticulata (SNr) ir vidiniuose bei išoriniuose globus pallidus segmentuose (smegenų dalis, reguliuojanti savanorišką judėjimą). Hipokampas, ypač dentato gyrus, ir smegenėlės taip pat turi didesnį CB1 receptorių tankį. Smegenų kamiene randama labai nedaug CB1 receptorių. Šios vietos rodo CB1 receptorių dalyvavimą moduliuojant atmintį, emocijas, skausmą ir judėjimą. Įrodyta, kad Δ9-THC, nukreiptas į CB1 receptorius, sumažina nociceptiją gyvūnų ūminio, visceralinio, uždegiminio ir lėtinio skausmo modeliuose. Pacientų tyrimuose su lėtiniu skausmu ir neuropatiniu skausmu marihuanos ar kanabinoidų ekstraktų vartojimas sukėlė teigiamus ir pagerėjusius simptomus.
Neuronų CB1 receptorių aktyvinimas slopina adenilo ciklazę ir sumažina neurotransmiterių išsiskyrimą blokuodamas įtampos valdomus kalcio kanalus. Šių signalizavimo kelių aktyvavimas CB1 receptoriais ir didelis šių receptorių kiekis presinaptiniuose terminaluose rodo, kad CB1 receptorių endokanabinoidinė stimuliacija slopina neuronų jaudrumą ir slopina neurotransmisiją. Dėl šių poveikių buvo tiriami fitokanabinoidai epilepsijai gydyti. Keletas farmacijos kompanijų bando sukurti sintetinius didelio afiniteto CB1 antagonistus ir atvirkštinius agonistus kaip terapinius vaistus diabetui, metaboliniam sindromui ir priklausomybei nuo narkotikų.CB2 receptoriai
CB2 receptoriai, skirtingai nei CB1, nėra labai išreikšti centrinėje nervų sistemoje (CNS). Δ9-THC poveikis imuninei funkcijai buvo priskirtas CB2 kanabinoidų receptorių sąveikai, daugiausia randamai imuninėse ląstelėse. CB2 receptoriai yra plačiai pasiskirstę pagrindiniuose imuninių ląstelių gamybos ir reguliavimo audiniuose, įskaitant blužnį, tonziles ir užkrūčio liauką. Šios ląstelių linijos apima B ir T limfocitus, natūralias žudikų ląsteles, monocitus, makrofagus, mikroglijos ląsteles ir putliąsias ląsteles. Kaip ir CB1 receptoriai, endokanabinoidų stimuliacija slopina CB2 receptorių neurotransmisiją.
Kultivuotų mikroglijos ląstelių tyrimas parodė, kad c-interferoną ir granulocitų makrofagų kolonijas stimuliuojantį faktorių (GM-CSF), žinomą kaip mikroglijos ląstelių uždegiminio atsako aktyvatorius, lydėjo reikšmingas CB2 receptorių reguliavimas. Tai rodo, kad CB2 receptoriai vaidina svarbų vaidmenį mikroglijos ląstelių funkcijoje CNS uždegiminiame atsake. CB2 aktyvinimas buvo susijęs su keliomis neurodegeneracinėmis ligomis, tokiomis kaip Huntingtono (HD) ir AD.Padidėjusi CB2 ekspresija smegenyse buvo patvirtinta naudojant CB2 selektyvias pozitronų emisijos tomografijos (PET) atsekamąsias medžiagas Alzheimerio pelių modeliuose. Ši padidėjusi ekspresija buvo susijusi su amiloido-beta plokštelių formavimu, o tai rodo galimą CB2 PET atsekamųjų medžiagų, kaip diagnostinio metodo nustatant neuroinflammacijos pradžią, naudingumą. CBD sąveika su CB2 receptoriais yra sudėtingesnė, tačiau, kaip ir Δ9-THC, manoma, kad CBD sumažina uždegiminį atsaką. CBD poveikis CB2 receptoriui yra tik vienas iš kelių būdų, kuriais CBD gali paveikti neuroinflammaciją . Kadangi tiek CBD, tiek Δ9-THC moduliuoja G baltymų sujungtų receptorių, susijusių su endokanabinoidų sistema, aktyvumą, o CBD gali veikti kaip dalinis agonistas ir antagonizuoja Δ9-THC, CBD didesnėmis dozėmis tam tikru mastu gali neutralizuoti psichoaktyvų Δ9-THC poveikį. Šį poveikį pastebi daugelis kanapių vartotojų, kurie kartu vartoja CBD.
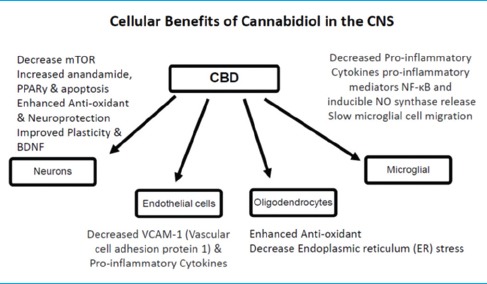
Skirtingai nuo psichoaktyviųjų savybių, susijusių su Δ9-THC, įrodyta, kad CBD turi labai mažą toksiškumą žmonėms ir kitoms rūšims. Prarytas ir absorbuojamas CBD greitai pasiskirsto ir dėl savo lipofilinio pobūdžio gali lengvai praeiti kraujo ir smegenų barjerą. Galutinis CBD pusinės eliminacijos laikas yra apie 9 val. ir pirmiausia išsiskiria su šlapimu kaip laisva ir gliukuronido forma.
CBD tyrimai su gyvūnų modeliais ir žmonėmis parodė daugybę terapinių savybių smegenų funkcijai ir apsaugai, tiek tiesiogiai veikiant ECS, tiek darant įtaką endogeniniams kanabinoidams. Apskritai, CBD parodė anksiolitinę, antidepresantinę, neuroprotekcinę priešuždegiminę ir imunomoduliacinę naudą. CBD sumažina uždegiminių citokinų gamybą, daro įtaką mikroglijos ląstelėms, kad jos grįžtų į ramią būseną, išsaugo smegenų kraujotaką išeminių įvykių metu ir sumažina kraujagyslių pokyčius bei neuroinflammaciją. Kitas CBD poveikis yra kalcio pernašos per membranas slopinimas, anandamido įsisavinimo ir fermentinės hidrolizės slopinimas bei indukuojamo NO sintazės baltymo ekspresijos ir branduolinio faktoriaus (NF)-κB aktyvacijos slopinimas. CBD padidina smegenų adenozino kiekį, sumažindamas adenozino reabsorbciją. Padidėjęs adenozinas yra susijęs su neuroprotekcija ir sumažėjusiu uždegimu po smegenų traumos. Taip pat žinoma, kad CBD daro poveikį kraujagyslėms, sukelia vazodilataciją, taip pat hipotenziją, kuri gali būti naudinga kaip apsauga nuo smegenų kraujagyslių pažeidimo, susijusio su insultu. CBD turi keletą savybių, kurios gali būti naudojamos AD gydymui, įskaitant glutamato sukelto sužadinimo prevenciją, uždegimą skatinančių mediatorių mažinimą ir gebėjimą pašalinti reaktyvias deguonies rūšis (ROS) ir sumažinti lipidų peroksidaciją. Eksperimentiškai, in vitro, kanabinoidų receptorių sąveika su CBD ir Δ9-THC, kartu ir atskirai, parodė neuronų apsaugą nuo sužadinimo, hipoksijos ir gliukozės trūkumo; In vivo kanabinoidai mažina hipokampo neuronų praradimą ir infarkto tūrį po smegenų išemijos, ūminės smegenų traumos ir sukelto ekscitotoksiškumo. Šis poveikis buvo priskirtas glutamato perdavimo slopinimui, kalcio antplūdžio sumažėjimui, sumažėjusiam mikroglijos aktyvavimui ir vėlesniam kenksmingų kaskadų slopinimui, pvz., Naviko nekrozės faktoriaus-alfa generavimui ir oksidaciniam stresui. Taip pat įrodyta, kad Δ9-THC apsaugo smegenis nuo įvairių neuronų pažeidimų ir pagerina neurodegeneracijos simptomus gyvūnų modeliuose MS, PD, HD, amiotrofinė šoninė sklerozė (ALS) ir AD. Kaip ir CBD, Δ9-THC gali pasiūlyti ne ECS apsaugą tiesioginiu poveikiu neuronų ląstelėms ir neneuroniniams elementams smegenyse. Mechanizmai apima sužadinimo glutamaterginių transmisijų ir sinapsinio plastiškumo moduliavimą, imuninio atsako moduliavimą, priešuždegiminių mediatorių išsiskyrimą, N-metil-D-aspartato receptorių jaudrumo moduliavimą ir jo poveikį tarpų sankryžoms, kalciui ir antioksidantams. AD būdingas padidėjęs beta-amiloido peptidų nusėdimas kartu su glialų aktyvacija senatvinėse plokštelėse, selektyvus neuronų praradimas ir pažinimo deficitas. Kanabinoidai yra neuroprotekciniai nuo ekscitotoksiškumo in vitro ir pacientams, sergantiems ūminiu smegenų pažeidimu. AD sergantiems žmonėms ląsteliniai senilinių plokštelių tyrimai parodė kanabinoidų receptorių CB1 ir CB2 ekspresiją kartu su mikroglijos aktyvacijos žymenimis. Tačiau kontrolinių CB1 teigiamų neuronų yra daugiau, palyginti su AD mikroglijos aktyvacijos sritimis. AD smegenyse taip pat pastebimai sumažėjo G-baltymų receptorių jungtis ir CB1 receptorių baltymų ekspresija. Paprastai manoma, kad aktyvuotas mikroglijos klasteris senatvinėse plokštelėse yra atsakingas už vykstantį uždegiminį ligos procesą.Šaltinis: Fitokanabinoidų neurologinės naudos apžvalga - PMC (nih.gov)
Dravet sindromas
2023-07-30,
Komentarų nėra
Dravet
sindromas – viena iš kūdikystėje prasidedančių retų
epilepsijos rūšių, susijusių su genetinėmis mutacijomis. Tai
yra viena iš sunkiausių vaistams atsparios epilepsijos formų
Šis sindromas dažniausiai prasideda viso kūno traukuliais
karščiavimo metu, kurie linkę užsitęsti iki epilepsinės būklės.
Vėliau traukuliai ar kitokie epilepsijos priepuoliai kartojasi be
karščiavimo.
Dravet
sindromas – sudėtingas ir vedantis į vaikų raidos regresą,
protinę ir fizinę negalią. Daugiau
nei 85 proc. Dravet sindromo atvejų lemia geno SCN1A mutacija. Šis
genas atsakingas už nervinėse ląstelėse esančių natrio kanalų
kodavimą. Apie 90 proc. genetinių mutacijų atsiranda savaime,
vaikai jų nepaveldi iš tėvų.
Lietuvoje
prieinamos alternatyvos Dravet sindromo gydymui – specifinis
vaistas stiripentolis, taip pat gydymas ketogenine dieta, kai
didžioji maisto kalorijų dalis gaunama iš riebalų. Kauno
klinikose šis metodas taikomas jau ketvirti metai. Pastaraisiais
metais Europos Sąjungoje šio labai reto sindromo gydymui įteisinti
dar du nauji vaistai – fenfluraminas ir CBD
(kanabidiolis).
______________________________________________________________
Šaltinis: Reta epilepsijos rūšis – klastingasis Dravet sindromas: kaip jį atpažinti ir gydyti (vlmedicina.lt)
cbd dravet syndrome - „Google“ mokslinčius